الرئيسية
أخبارعاجلة
رياضة
- أخبار الرياضة الإماراتية والعربية والعالمية
- أخبار الرياضة والرياضيين
- فيديو اخبار الرياضة
- نجوم الملاعب
- أخبار الرياضة
- ملاعب
- بطولات
- أندية الإمارات
- حوارات وتقارير
- رياضة عربية
- رياضة عالمية
- موجب
- سالب
- مباريات ونتائج
- كرة الطائرة
- كرة اليد
- كرة السلة
- رمي
- قفز
- الجري
- تنس
- سيارات
- غولف
- سباق الخيل
- مصارعة
- جمباز
- أخبار المنتخبات
- تحقيقات
- مدونات
- جمباز
ثقافة
إقتصاد
فن وموسيقى
أزياء
صحة وتغذية
سياحة وسفر
ديكور
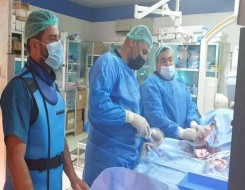
"الصحة" تحذر من استخدام Brilinta 90 mg لعلاج النوبات القلبية

وزارة الصحة ووقاية المجتمع الإماراتية
دبي - صوت الإمارات
أعلنت وزارة الصحة ووقاية المجتمع الإماراتية، أنها أصدرت تعميماً إلى المناطق الطبية والمستشفيات بسحب تشغيلة واحدة من المنتج الدوائي Brilinta 90 mg والتي تحمل الرقم: JB504، والمستخدمة لدى المرضى الذين يعانون النوبة القلبية والسكتة الدماغية، وذلك لأن عبوة المنتج تحتوي على دواء آخر يسمى (Zurampic (lesinurad) 200mg tablet)، والذي يتم تصنيعه أيضاً من قبل شركة (AstraZeneca).
وأشار الدكتور أمين حسين الأميري الوكيل المساعد لسياسة الصحة العامة والتراخيص رئيس اللجنة العليا لليقظة الدوائية إلى أن إدارة الغذاء والدواء الأمريكية قد أصدرت تحذيراً يفيد بأن الشركة المصنعة للمنتج المذكور قامت طوعاً بسحب تشغيلة واحدة، حيث إن الجرعات غير المعتمدة من دواء Zurampic قد تؤدي إلى حدوث آثار سلبية كلوية مثل الفشل الكلوي، والتوقف المفاجئ من استخدام دواء Brilinta قد يزيد من خطر الإصابة بالنوبة القلبية والسكتة الدماغية.
وتم اعتماد هذا المنتج من قبل إدارة الغذاء والدواء الأمريكية، وهو يمنع تجلط الدم في الأوعية الدموية والنوبات القلبية في المرضى الذين يعانون متلازمة الشريان التاجي الحادة (ACS).
GMT 16:53 2024 الجمعة ,09 شباط / فبراير
الذهاب للعمل مشي يقلل من خطر النوبات القلبيةGMT 21:58 2020 الثلاثاء ,03 آذار/ مارس
إليك الفرق بين السكتة الدماغية والسكتة القلبية وسكتة العينGMT 21:12 2019 الأحد ,22 كانون الأول / ديسمبر
"الكوليسترول" الارتفاع الحاد يزيد مخاطر الإصابة بالنوبات القلبيةGMT 21:53 2019 الجمعة ,25 كانون الثاني / يناير
تناول أدوية علاج الإنفلونزا قد يصيك بأمراض خطيرة في القلب والدماغGMT 16:14 2016 الأربعاء ,12 تشرين الأول / أكتوبر
الإجهاد الجسدي والانزعاج العاطفي من مسببات نوبات القلبصندوق النقد يتوقع نمو اقتصاد الإمارات بنسبة 5.1% في 2025
دبي - صوت الإمارات
أبقى صندوق النقد الدولي على توقعاته بنمو إجمالي الناتج المحلي الإجمالي لدولة الإمارات بنسبة 4 بالمئة في العام 2024، ومن ثم ترتفع إلى 5.1 بالمئة خلال العام القادم 2025.وتوقع الصندوق في تقرير آفاق الاقتصاد العالمي الصادر �...المزيدأصالة تحتفل بفوزها بجائزة "جوي أوورد" للعام الثاني وتستعد لإهداء الجمهور أغنية جديدة "ممنوع"
الرياض - صوت الإمارات
الفنانة أصالة خطفت الأنظار في حفل توزيع جوائز "جوي أوورد" بعدما فازت بجائزة المغنية المفضلة للعام الثاني على التوالي، وعاشت الفنانة أصالة عام مليء بالإنجازات والأعمال الفنية المتنوعة والتي جعلتها تستحق الفو�...المزيدماسك يحذر من "هلوسة" الذكاء الاصطناعي بسبب نفاد البيانات على الإنترنت
واشنطن - صوت الإمارات
في تحذير جديد أطلقه إيلون ماسك، مؤسس شركة تسلا وSpaceX، حذر من خطر "هلوسة الذكاء الاصطناعي" في المستقبل القريب، وذلك بسبب احتمالية نفاد البيانات المتاحة على الإنترنت لتدريب الأنظمة الذكية. وتوقع ماسك أن الذكاء ا�...المزيدبرنامج أمير الشعراء يختتم المرحلة الأولى في موسمه الـ11 ويعلن عن المتأهلين
أبوظبي ـ صوت الإمارات
اختتم برنامج أمير الشعراء، الذي تنتجه هيئة أبوظبي للتراث، المرحلة الأولى من موسمه الحادي عشر، بالحلقة المباشرة الخامسة التي بُثت مساء أمس الخميس 2 يناير 2025، وذلك من على مسرح شاطئ الراحة في أبوظبي.وخلال هذه الحلقة ت...المزيدنجم منتخب البرازيل وريال مدريد فينيسيوس جونيور يفوز بجائزة الأفضل لعام 2024
الدوحة - صوت الإمارات
حصد النجم البرازيلي فينيسيوس جونيور، مهاجم ريال مدريد، جائزة أفضل لاعب في العالم لعام 2024، خلال حفل الاتحاد الدولى لكرة القدم "فيفا" المقام مساء الثلاثاء، للكشف عن الفائزين بـ جوائز The Best من فيفا لعام 2024 وأبرزه�...المزيدأحلام بإطلالات ناعمة وراقية في المملكة العربية السعودية
الرياض - صوت الإمارات
النجمة الإماراتية أحلام الشامسي كشفت أخيرًا عن ألبومها الجديد لعام 2025، وأفرجت الفنانة أحلام عن أولى اللقطات من كواليس وتحضيرات ألبومها الجديد، ونشرت فيديو عبر حسابها بانستجرام شوقت به الجمهور لأعمالها ومفاجآتها الفنية الجديدة من خلال الألبوم الجديد، وكتبت أحلام في تعليقها على برومو الكليب الجديد الذي بصدد طرحه قريبًا: "أحلام 2025" والذي تكهن البعض أنه سيكون عنوان ألبومها الجديد، بالإضافة إلى تعليقها على الفيديو "صنع في السعودية"، حيث اعتبر البعض أن تلك إشارة إلى أن أحلام صنعت ألبومها الجديد بالكامل في السعودية، وبالتزامن مع تلك المناسبة دعونا نرصد أجمل إطلالات النجمة أحلام خلال الفعاليات والحفلات التي حضرتها في المملكة العربية السعودية. إطلالات ناعمة وراقية من وحي النجمة أحلام في السعودية في حفل زفاف سابق قامت...المزيد Maintained and developed by Arabs Today Group SAL
جميع الحقوق محفوظة لمجموعة العرب اليوم الاعلامية 2023 ©
Maintained and developed by Arabs Today Group SAL
جميع الحقوق محفوظة لمجموعة العرب اليوم الاعلامية 2023 ©
























أرسل تعليقك